Фенолы - это соединения, в молекулах которых содержится ароматическое (бензольное) кольцо, связанное с одной или несколькими группами -ОН. Большое содержание фенолов характерно для растительной клетки.
В животном организме бензольные кольца не синтезируются, а могут только преобразовываться, поэтому они должны постоянно поступать в организм с пищей. При этом многие фенольные соединения в животных тканях выполняют важные функции (убихинон, адреналин, тироксин, серотонин и др.).
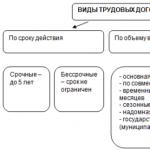
Сегодня в растениях уже найдено несколько тысяч разнообразных фенольных соединений. Их классифицируют по строению углеродного скелета:
1. С 6 -фенолы
2. С 6 -С 1 -фенольные кислоты
3. С 6 -С 3 -гидроксикоричные кислоты и кумарины
4. С 6 -С 3 -С 6 -флавоноиды
5. Олигомерные фенольные соединения.
6. Полимерные фенольные соединения.
С 6 -Фенолы. Соединения, бензольное кольцо которых связано с несколькими гидроксильными группами, называют полифенолами.
Свободные фенолы в растениях встречаются редко и в малых количествах. Так, фенол обнаружен в иглах и шишках сосны, в эфирном масле черной смородины, пирокатехин - в чешуе лука, в листьях бадана, гидрохинон - в коре и листьях груши, в листьях бадана. Чаще встречаются произ-водные фенолов, где они связаны с какой-либо углеродной цепью или циклом. К примеру, урушиол и тетрагидроканнабинол.
Урушиол - это токсическое вещество из листьв сумаха. Тетрагидроканнабинол является галлюциногенным началом конопли.
При окислении фенолов образуются хиноны (бензохиноны). В свободном состоянии хиноны в растениях не встречаются, зато распространены их производные. К примеру, производными бензохинонов являются переносчики электронов в ЭТЦ фотосинтеза и дыхания - пластохинон и убихинон. К производным бензохинона относятся также жгучее вещество примулы - примин и красный пигмент мухомора - мускаруфин.
С 6 -С 1 -фенольные кислоты. В растениях распространены фенольные кислоты. Чаще они находятся в тканях в связанном состоянии и освобождаются при выделении и гидролизе.
Салициловая кислота выделяется в качестве аллелопатического агента в окружающую среду. Вместе с тем, в настоящее время обнаружено ее регулирующее действие на ряд физиологических и биохимических процессов в растении (образование этилена, восстановление нитратов и др.).
Протокатеховая кислота обнаружена в чешуях лука.
Ванильная и галловая кислоты встречаются в древесине. Последняя входит в состав некоторых дубильных веществ и может образовывать диме-ры - дигалловую кислоту, в молекуле которой сложноэфирной связью соединены 2 остатка галловой кислоты.
Обнаружены в растениях производные фенольных кислот - альдегиды и спирты. К примеру, в коре ивы присутствует салициловый спирт. Но особенно известен ванилин - ванильный альдегид. Он обладает очень приятным запахом и в виде гликозида - глюкованилина содержится в плодах и ветвях ванильного дерева. Гликозид и сам ванилин широко применяются в кондитерской, мыловаренной и парфюмерной промышленности.
Фенольные кислоты могут связываться сложноэфирными связями с сахарами, чаще с глюкозой. Из ряда растений (ревень, эвкалипт) выделен гликогаллин, в котором карбоксильная группа галловой кислоты связана с гликозидным гидроксилом глюкозы.
С 6 -С 3 -гидроксикоричные кислоты и кумарины. Широко распространены в растениях гидроксикоричные кислоты. Обычно они находятся в связанном состоянии, а в свободном, кроме кофейной, встречаются редко.
Показано, что цис-изомеры гидроксикоричных кислот являются активаторами ростовых процессов растений, а транс-изомеры такими свойствами не обладают.
В растениях встречаются гидроксикоричные спирты - производные соответствующих кислот: кумаровой - кумаровый спирт, феруловой - ко-нифериловый спирт, синаповой - синаповый спирт. Спирты обычно не накапливаются, а, очевидно, используются на образование лигнина, мономерами которого они являются.
Гидроксикоричные кислоты могут образовывать сложные эфиры с органическими кислотами алифатического ряда. Так, кофейная кислота образует эфиры с яблочной и винной кислотами. Первый эфир называют фазеолиновой кислотой. Она присутствует в листьях фасоли. Второй - цикориновой кислотой. Она найдена в листьях цикория.
В растениях распространены эфиры гидроксикоричных кислот и сахаров, чаще глюкозы. Так, в цветках петунии и львиного зева обнаружены эфиры кофейной, кумаровой, феруловой кислот, а в злаках вообще большинство гидроксикоричных кислот представлены эфирами. Вместе с тем, гидро-ксикоричные кислоты входят в состав полисахаридов и белков. К примеру, феруловая кислота найдена в ксиланах пшеничной муки и в полисахаридах ананасов.
Кумарины - это лактоны, которые образуются при замыкании кольца между гидроксильной и карбоксильной группами в молекуле гидроксико-ричной кислоты.
Кумарин - бесцветное кристаллическое вещество с приятным запахом свежескошенного сена. В свободном виде кумарин в растениях не встречается. Он обычно содержится в виде гликозидов (цветы и листья донника). У травянистых растений в клеточном соке присутствует гликозид, содержа-щий орто-кумаровую кислоту. При сенокосе растительные ткани повреждаются, нарушается проницаемость мембран. Гликозиды из клеточного сока соприкасаются с ферментами цитоплазмы. От гликозидов отщепляются сахара, и кумаровая кислота после транс-цис-изомеризации замыкается в лактон-кумарин. При этом вянущая трава приобретает запах сена.
В растениях часто встречаются гидроксилированные кумарины в составе гликозидов. К примеру, эскулетин из околоплодника конского каштана и скополетин из корней скополии японской. Оба эти кумарина обладают Р-витаминной активностью и используются в медицине как капилляроукрепля-ющие средства.
В доннике белом найден дикумарин, который препятствует свертыванию крови. Этот и другие дикумарины используются как лекарственные препараты, предотвращающие образование тромбов.
С 6 -С 3 -С 6 -флавоноиды . Это одна из наиболее разнообразных и распространенных групп фенольных соединений. В корне строения молекул флавоноидов лежит структура флавана, который состоит из двух бензольных колец и одного гетероциклического (пиранового).
Флавоноиды делят на несколько групп.
1. Катехины.
2. Антоцианы.
3. Халконы.
Катехины - наиболее восстановленные флавоноиды. Οʜᴎ не образуют гликозидов. Катехин впервые был выделен из древесины Acacia catechu, отсюда его название. Катехины найдены у более чем 200 видов растений. Среди катехинов наиболее известны катехин и галлокатехин.
Οʜᴎ могут образовывать эфиры с галловой кислотой - катехингаллаты и галлокатехингаллаты. Катехины содержатся во многих плодах (яблоки, груши, айва, вишни, сливы, абрикосы, земляника, ежевика, смородина, брусника, виноград), в бобах какао, зернах кофе, в коре и древесине многих деревьев (ива, дуб, сосна, пихта͵ кедр, кипарис, акация, эвкалипт). Особенно много катехинов в листьях и молодых побегах чая (до 30%). Окислительные превращения катехинов играют важную роль в чайном производстве и виноделии. Продукты окисления, а это в основном димеры катехинов, имеют приятный слабовяжущий вкус и золотисто-коричневую окраску. Это определяет цвет и вкусовые качества конечного продукта. При этом катехины обладают высокой Р-витаминной активностью, укрепляют капилляры и нормализуют проницаемость стенок сосудов. Такой же активностью обладают и димеры катехинов в чае. Катехины в качестве мономеров входят в состав конденсированных дубильных веществ.
Антоцианы - важнейшие пигменты растений. Οʜᴎ окрашивают лепестки цветков, плоды, иногда листья в голубой, синий, розовый, красный, фиолетовый цвета с различными оттенками и переходами. Все антоцианы - гликозиды. Их агликонами являются антоцианидины. Антоцианы растворимы в воде и содержатся в клеточном соке.
Сегодня известно более 20 антоцианидинов, но наиболее широко распространены 4: пеларгонидин, цианидин, дельфинидин и мальви-дин (метилированное производное дельфинидина).
В качестве моносахаридов в антоцианах встречаются глюкоза, галактоза, рамноза, ксилоза, реже арабиноза, а в качестве дисахаридов - чаще всего рутиноза, софороза, самбубиоза. Иногда антоцианы содержат трисахариды, обычно разветвленные. К примеру, в ягодах смородины и малины найден антоциан, в котором с цианидином связан разветвленный трисахарид.
Окраска антоцианов зависит от ряда факторов:
1. концентрации антоцианов в клеточном соке;
2. рН клеточного сока;
3. комплексообразования антоцианов с катионами;
4. копигментации - смеси антоцианов и присутствия в клеточном соке других веществ фенольной природы;
5. сочетания с окраской пластидных пигментов.
Рассмотрим эти факторы подробнее.
1. Концентрация антоцианов в клеточном соке может меняться в широком диапазоне - от 0,01 до 15%. К примеру, в обычном синем васильке содержится 0,05% антоциана цианина, а в темно-пурпурном его 13-14%.
2. По причине того, что в молекулах антоциана имеется свободная валентность, окраска может меняться исходя из величины рН. Обычно в кислой среде антоцианы имеют красный цвет различной интенсивности и оттенков, а в щелочной - синий. Такие изменения в окраске антоцианов можно наблюдать, добавляя кислоту или щелочь к окрашенному соку смородины, вишни, столовой свеклы или краснокачанной капусты. В природе же резких изменений рН клеточного сока не происходит, и данный фактор в окраске антоцианов большой роли не играет. Можно только заметить, что некоторые розовые и красные цветы при завядании синеют. Это указывает на изменение рН в отмирающих клетках.
3. Большое значение в окраске цветков и плодов имеет способность антоцианов к хелатообразованию с ионами металлов. Это хорошо видно на примере василька и розы. В их лепестках содержится один и тот же антоциан - цианин. В лепестках синего василька цианин образует комплекс с ионами Fe (4 молекулы цианина связаны с одним атомом Fe). В лепестках красных роз присутствует свободный цианин. Другой пример.
Размещено на реф.рф
В случае если обычную гортензию с розовыми цветками выращивать на минеральной среде, содержащей алюминий и молибден, то цветки приобретают синюю окраску.
4. Обычно в клеточном соке многих цветков и плодов присутствует не один, а несколько пигментов. При этом окраска зависит от их смеси, и ее называют копигментацией. Так, окраска плодов черники обусловлена копигментацией дельфинина и мальвина. В фиолетовых цветках картофеля найдено 10 различных антоцианов.
Цветовой рисунок лепестков многих цветков определяется или локальным увеличением концентрации одного пигмента (наперстянка), или наложением дополнительного пигмента на основной (в центре цветков мака на общем фоне пеларгонина накладывается высокая концентрация цианина).
На окраску влияет также копигментация антоцианов с другими веществами, к примеру, с таннинами. Так, пурпурные и темно-красные розы содержат один и тот же цианин, но у темно-красных он копигментирован с большим количеством таннина.
5. При сочетании синих антоцианов клеточного сока и желто-оранжевых каротиноидов хромопластов получается коричневая окраска лепестков некоторых цветков.
Табл. Некоторые антоцианы растений
| Антоциан | Агликон | Сахар | Растения |
| Пеларгонин | Пеларгонидин | 2 глюкозы | Пеларгония, астры |
| Цианин | Цианидин | 2 глюкозы | Розы, васильки |
| Керацианин | Цианидин | Глюкоза, рамноза | Вишни |
| Пруницианин | Цианидин | Рамноза, глюкоза | Сливы |
| Идаин | Цианидин | Галактоза | Брусника |
| Хризантемин | Цианидин | Глюкоза | Астры, черника, бузина |
| Мальвин | Мальвидин | 2 глюкозы | Мальва |
| Энин | Мальвидин | Глюкоза | Виноград |
| Дельфиний | Дельфинидин | Рамноза, глюкоза | Шпорник |
| Вигланин | Дельфинидин | Глюкоза, рамноза | Мать-и-мачеха |
Халконы , или антохлоры, - это флавоноиды с раскрытым гетероциклом. Οʜᴎ придают лепесткам цветков желтую окраску. Их распространение ограничено девятью семействами. Встречаются они в виде гликозидов. Халконами, к примеру, являются изосалипурпозид из желтых цветков гвоздики, флоридзин из коры и листьев яблони. Флоридзин является ингибитором роста яблони. При приеме внутрь человеком он вызывает одноразовое интенсивное выделение глюкозы в кровь - ʼʼфлоридзиновый диабетʼʼ.
Олигомерные фенольные соединения. Сюда относятся лишайниковые кислоты. Οʜᴎ образуются в лишайниках из двух и более остатков орселлиновой кислоты. Леканоровая и эверновая кислоты состоят из двух остатков орселлиновой кислоты. Эверновая кислота - основной компонент комплекса кислот эвернии (ʼʼдубовый мохʼʼ), который используется в парфюмерии как душистое вещество и одновременно как фиксатор при изготовлении лучших сортов духов.
Среди лишайниковых кислот есть окрашенные. Οʜᴎ придают разнообразный цвет лишайникам - желтый, оранжевый, красный, фиолетовый. Лишайник уснея содержит усниновую кислоту, которая является эффективным бактерицидным средством.
Встречаются в коре, древесине, плодах и листьях многих растений димеры гидроксикоричных спиртов. Образуют олигомеры и флавоноиды, особенно катехины. Димеры катехина найдены в яблоках, каштанах, боярышнике, бобах какао, в древесине эвкалипта.
Полимерные фенольные соединения. К полимерным фенольным соединениям относятся дубильные вещества, или таннины, лигнины и меланины.
Дубильные вещества, или танины. Свое название они получили благодаря способности дубить шкуру животных, превращая ее в кожу. Дубление основано на взаимодействии дубильных веществ с белком кожи -коллагеном. При этом образуются многочисленные водородные связи между белком и таннином.
Природные дубильные вещества представляют из себясложную смесь близких по составу соединений с молекулярной массой 500-5000.
Много дубильных веществ содержится в коре и древесине дуба, эвкалипта͵ древесине каштана, в корневище щавеля, ревеня, в листьях сумаха. Их много в коре и древесине бобовых, миртовых, розовых. Особенно высоким содержанием дубильных веществ отличаются галлы, которые образуются на листьях при повреждении их орехотворкой (до 50-70%).
Дубильными (чаще пищевыми дубильными) называют также более низкомолекулярные вещества, обладающие приятным вяжущим вкусом, но не способные к настоящему дублению. Οʜᴎ присутствуют во многих плодах (айва, яблоки, хурма, виноград), в листьях чая.
Дубильные вещества находят самое широкое применение не только в кожевенной промышленности. Их используют в производстве пластмасс, связующих веществ при изготовлении фанеры и плит из опилок, в качестве протравы при крашении. Οʜᴎ находят применение в установках для кипячения воды в качестве стабилизаторов коллоидов, для регулирования вязкости растворов при бурении скважин.
Использование таннинов в виноделии связано с их ингибирующим действием на ферменты и микроорганизмы, что предотвращает помутнение вин и улучшает их качество. С помощью чайного таннина стабилизируют бетацианин - пищевой красный краситель, получаемый из столовой свеклы.
В медицине дубильные вещества применяются как вяжущие, бактерицидные, противолучевые и противоопухолевые средства.
Лигнин входит в состав клеточных оболочек тканей древесины. Он откладывается между микрофибриллами целлюлозы, что придает клеточным оболочкам твердость, прочность. При этом при этом нарушается связь между клетками, что приводит к отмиранию живого содержимого, в связи с этим лиг-нификация является заключительным этапом онтогенеза клетки.
Лигнин - аморфное вещество, нерастворимое в воде, органических растворителях и даже в концентрированной кислоте.
Лигнин имеет еще одно важное свойство: он устойчив к микроорганизмам. Лишь немногие микроорганизмы, и то очень медленно, разлагают его.
Лигнин - трехмерный полимер, мономерами которого являются гидроксикоричные спирты. Так, у хвойных в лигнине преобладает ко-нифериловый спирт, у злаков - кумаровый, у многих лиственных деревьев - синаповый.
В целлюлозно-бумажной промышленности и на гидролизных заводах накапливается в качестве отходов большое количество лигнина. Его используют для получения активированного угля, пластмасс, синтетических смол.
Меланины - полимеры фенольной природы, которые являются продуктом окисления тирозина. Их строение еще до конца не выяснено.
Меланины имеют черный или коричнево-черный цвет. Их образованием объясняется быстрое потемнение поверхности разрезанного яблока, клубня картофеля, некоторых грибов. Меланины присутствуют и в животных организмах, обусловливая окраску шерсти и волос. При этом растительные и животные меланины отличаются по составу мономеров. Растительные меланины при гидролизе образуют пирокатехин, а животные - дигидроксииндол. Иными словами, растительные меланины, в отличии от животных являются безазотистыми веществами.
Функции фенольных соединений в растении. 1. Фенолы участвуют в окислительно-восстановительных процессах: происходит превращение фенолов в хиноны и наоборот с участием фермента полифенолоксидазы. При этом попутно неферментативным путем могут окисляться различные соединения (аминокислоты, органические кислоты, фенолы, цитохромы и др.).
2. Некоторые фенольные соединения являются переносчиками электронов и протонов в ЭТЦ фотосинтеза и дыхания (пластохинон, убихинон).
3. Ряд фенолов оказывает влияние на ростовые процессы растений, иногда активирующее, чаще ингибирующее. Это влияние бывает опосредовано действием на фитогормоны. Так, известно, что одни фенольные соединения необходимы при синтезе ауксина, другие - при его распаде. Для образования этилена крайне важно присутствие эфира кумаровой кислоты. Установлено, что при стрессе растения накапливают большое количество фе-нолов, что приводит к ингибированию ростовых процессов и повышению их устойчивости к неблагоприятным условиям.
4. Фенолы выполняют в растениях защитную функцию: Фенольные соединения придают растениям устойчивость к заболеваниям. К примеру, устойчивость к ряду болезней лука с окрашенной шелухой связана с присутствием в нем протокатеховой кислоты. При механических повреждениях растительных тканей в клетках накапливаются фенолы и, конденсируясь, образуют защитный слой. Некоторые растения в ответ на поражение патогенными грибами образуют защитные вещества - фитоалексины, многие из которых имеют фенольную природу.
5. Многие фенолы являются антиоксидантами и защищают липиды мембран от окислительного разрушения. Некоторые из них используют в пищевой промышленности для предохранения жиров от прогоркания (эфиры галловой кислоты, флавоноиды и др.).
6. Очень важна роль фенольных соединений в процессе размножения растений. Это не только связано с окраской цветков и плодов, но и с непосредственным участием фенолов в оплодотворении. Так, в процессе оплодотворения водоросли хламидомонады и высшего растения форзиции принимают участие флавоноиды.
7. Фенолы могут выступать у некоторых растений в качестве аллелопатических веществ. Например, таким веществом у дуба должна быть салициловая кислота.
8. Некоторые фенолы действуют как активаторы или ингибиторы на отдельные процессы и ферменты (деление клеток, синтез белка, окислительное фосфррилирование и т. д.).
Фенольные соединения - понятие и виды. Классификация и особенности категории "Фенольные соединения" 2017, 2018.
Фенольные соединения, т. е. производные фенола, которых насчитывается свыше тысячи в растительных продуктах, играют важную биологическую роль в клетках и тканях растений. В растительных продуктах они находятся в свободном состоянии, а чаще в связанной форме. Фенольные соединения обусловливают устойчивость плодов и овощей к фитопатогенным микроорганизмам, придают вкус, аромат и окраску продуктам.
К фенольным соединениям относятся: салициловая и бензойная кислоты, кофейная кислота, которая находится в кофе; хинная кислота, обнаруженная в яблоках, винограде, чернике, клюкве и сливах; хлорогеновая кислота, молекула которой состоит из двух бензольных колец - остатков хинной и кофейной кислот, соединенных по типу сложных эфиров.
Хлорогеновая кислота участвует в процессах внутриклеточного дыхания: она легко окисляется и восстанавливается. Ее окисленная форма - хинон - обладает сильной защитной реакцией от микроорганизмов. Хлорогеновая кислота распространена в растениях, найдена в картофеле, яблоках и др.
Полиоксифенольные соединения с молекулярной массой 600-2000 принято называть дубильными веществами.
Дубильные вещества
Дубильные вещества находятся в плодах, овощах, чае, кофе и др. Наиболее богаты ими чай зеленый (от 10 до 30%) и черный (от 5 до 17% в пересчете на сухое вещество), терн (1,7%), хурма (до 2%), кизил, айва (0,6%), черная смородина (0,4%) и др. Терпкий, вяжущий вкус чая, черемухи, терна, хурмы обусловливается содержанием в них дубильных веществ.
Из дубильных веществ в пищевых продуктах преобладают гидролизуемые, или танины, и конденсированные, или катехины.
Гидролизуемые дубильные вещества - сложные эфиры, образованные углеводами (чаще всего глюкозой) и цепочкой фенолкарбоновых кислот (галловой, метадигалловой, протокатеховой и др.), соединенных между собой через атомы кислорода.
Танины легко гидролизуются под действием фермента таназы или кислот, с солями окиси железа дают темно-синее окрашивание. Гидролизуемые дубильные вещества находятся в чае, кофе и др.
Галловая и протокатеховая кислоты в свободном виде обнаружены в некоторых плодах. Конденсированные дубильные вещества - соединения, в молекулах которых фенольные (ароматические) ядра соединены через атомы углерода. В отличие от гидролизуемых дубильных веществ конденсированные дубильные вещества при нагревании с разбавленными кислотами подвергаются дальнейшему уплотнению. Их называют катехинами.
К ним относится не только катехин, но его изомеры (эпикатехины) и производные: сложные эфиры катехинов и галловой кислоты (катехингаллаты, галлокатехингаллаты, эпикатехингал- латы и др.). Катехины - бесцветные соединения, легко окисляются, с солями железа дают темно-зеленое окрашивание.
Дубильные вещества растворимы в воде, осаждают белки из растворов. На последнем свойстве дубильных веществ основано осветление вин: белки с дубильными веществами образуют нерастворимые соединения, которые захватывают взвешенные в вине частицы и оседают с ними на дно. Этим же объясняется ощущение «вяжущего» вкуса свободных дубильных веществ.
Дубильные вещества дают нерастворимые осадки со свинцовыми солями и алкалоидами. Поэтому при отравлении организма алкалоидами как противоядие вводят дубильные вещества.
Под действием фермента полифенолоксидазы хлорогеновая кислота и дубильные вещества окисляются, образуя коричневого и красного цвета аморфные вещества, называемые флобафенами. Образованием флобафенов обусловливается в основном цвет настоя чая, потемнение мякоти нарезанных плодов.
Для предупреждения потемнения нарезанных плодов и овощей инактивируют полифенооксидазу прогреванием сырья острым паром (при изготовлении сушеных овощей и компотов) или блокируют активную часть фермента, обрабатывая сырье сернистым ангидридом (при производстве сушеных плодов).
Дубильные вещества участвуют в образовании аромата продуктов. Например, при производстве чая происходит окислительное дезаминирование аминокислот чайного листа хинонами (первичными продуктами окисления катехинов), в результате чего образуются альдегиды, которые сами или продукты их превращения образуют аромат чая.
Дубильные вещества способствуют более длительной сохраняемости продуктов (вин, пива и др.), так как обладают бактерицидными свойствами. К фенольным соединениям относятся антоцианы, флавоны, флавонолы, придающие окраску плодам и овощам.
Смотрите также:

 Лекция № 4. Лекарственные растения и сырье, содержащие фенольные соединения.
Лекция № 4. Лекарственные растения и сырье, содержащие фенольные соединения.
Лекарственные растения и сырье, содержащие фенольные соединения Лекарственные растения и сырье, содержащие простые фенолы и фенологликозиды
План лекции
1.Классификация фенольных соединений
2Лекарственные растения и сырье, содержащие простые фенолы и
3.Лекарственные растения и сырье, содержащие фенологликозиды
Фенольные соединения - вещества ароматической природы, содержащие одну или несколькогидроксильных групп, связанных с атомами углерода ароматического ядра. Фенольные соединения, в ароматическом кольце которых имеется больше одной гидроксильной группы, называют полифенолами. Число природных фенольных соединений растительного происхождения оказалось настолько большим, а функции их настолько многообразны, что их изучение требует привлечения широкого круга исследователей.
В настоящее время доказано, что все полифенолы, за небольшим исключением, являются активными метаболитами клеточного обмена и играют существенную роль в различных физиологических процессах - фотосинтезе, дыхании, росте, устойчивости растений к инфекционным болезням. О важной биологической роли полифенолов свидетельствует характер их распределения в растении. Большая часть их содержится в активно функционирующих органах - листьях, цветках (придают окраску цветкам), плодах, проростках, в покровных тканях , выполняющих защитные функции. Разные органы и ткани отличаются не только количеством полифенолов, но и качественным их составом.
Из схемы видно , что биосинтезу многих групп фенольных соединений (в том числе флавоноидов, кумаринов и др.) предшествует образование аминокислот - L-фенилаланина и L-тирозина. На схеме показано также место образования некоторых витаминов (К, токоферолы).
Классификация фенольных соединений строится с учетом основного углеродистого скелета - числа ароматических колец и атомов углерода в боковой цепи. По этим признакам фенольные соединения подразделяются на группы:
Простые фенолы
Простые фенолы встречаются в растениях нечасто, и их распространение с точки зрения систематики носит случайный характер. Сам фенол обнаружен в иглах и шишках Pinus sylvestris, эфирных маслах листьев Nicotianatabacum, Ribes nigrum, лишайнике Evemia prunastri и др. Пирокатехин (1,2-ди-оксибензол) найден в листьях эфедры , чешуе лука, плодах грейпфрута. О содержании резорцина в растениях сведений не имеется.
Из диоксибензолов наиболее распространен гидрохинон (1,4-диоксибен-зол). Его гликозид арбутин присутствует в представителях следующих семейств: Ericaceae (Arctostaphylos, Rhododendron); Vacciniaceae(Vaccinium); Rosaceae (Pyrus, Docynia); Saxifragaceae (Bergenia); Asteraceae (Xanthium).
Метиловые и этиловые эфиры гидрохинона найдены в семействах Ру-rolaceae - Pyrola; Liliaceae -Hyacinthus; Illiciaceae - Illicium.
Из триоксибензолов в растениях встречается флороглюцин (1,3,5-триок-сибензол). В свободном виде он обнаружен в шишках Sequoia sempervirens и чешуе Allium сера, а в виде гликозида флорина - в околоплоднике плодов разных видов Citrus. Особое место занимают некоторые папоротники. В них накапливаются значительные количества производных флороглюцина, получивших общее название флороглюциды. В состав молекулы флороглюци-дов , кроме флороглюцина (большей частью метилированного), входит масляная кислота.
Листья толокнянки - Folia Uvae ursi
Растение. Толокнянка обыкновенная, или медвежье ушко, - Arctostaphy-los uva-ursi (L.) Spreng.; семейство вересковые - Ericaceae
Вечнозеленый, ветвистый, стелющийся кустарник или кустарничек. Листья небольшие, темно-зеленые, кожистые. Цветки розоватые, поникшие, собранные в короткие верхушечные кисти. Чашечка и венчик 5-зубчатые; венчик кувшинчатый, спайнолепестный. Плоды - красные, ягодообразные ценокарпные многокостянки с остающейся чашечкой, с 5 косточками в мучнистой, несъедобной мякоти. Цветет во второй половине апреля - мае; ягоды созревают к августу.
Распространена в лесной зоне европейской части России и Балтии, в Западной Сибири и реже на Дальнем Востоке
Химический состав. В
листьях содержится 8-16 % гликозидов - арбутин (гидрохинон-глюкозид), метиларбутин, свободный гидрохинон, галловая кислота, эллаговая кислота и флавоноиды, среди которых гиперозид.
Листья имеют обратнояйцевидную или узкообратнояйцевидную форму, к основанию суженные, короткочерешковые, цельнокрайние, сверху блестящие, темно-зеленые, голые, верхняя поверхность листа с сетью вдавленных жилок; с нижней стороны немного светлее, матовые, голые. Длина листьев около 2 см, ширина около 1 см. Желтые или почерневшие листья - признак окисления и других деструкции арбутина, метиларбутина и дубильных веществ.
В качестве примесей в пределах допустимого количества (не более 0,5 %) в сырье могут встречаться листья брусники, голубики, черники, которые легко распознаются по внешним признакам. Листья голубики (Vacciniumuliginosum L.) шире листьев толокнянки, овально-яйцевидной формы, цельнокрайние, некожистые и неблестящие; черники (Vaccinium myrtillus L.) - яйцевидные, тонкие с мелкозубчатым краем, светло-зеленые с обеих сторон . ГФ XI предусматривает цельное и измельченное сырье, в котором должно быть не менее 6 % арбутина.
Применение. Листья применяют в форме отваров при воспалительных заболеваниях мочевого пузыря и мочевых путей. Лечебное (антисептическое) действие обусловливается гидрохиноном, освобождающимся в организме при гидролизе арбутина и метиларбутина под действием ферментов и кислот. Раздражая почечный эпителий, арбутин оказывает также мочегонное действие. Лечебный эффект усиливается специфическим действием дубильных веществ и продуктов их гидролиза. Входит в состав мочегонных сборов.
Листья брусники - Folia Vitis idaeae
Растение. Брусника - Vaccinium vitis idaea L.; семейство брусничные - Vacciniaceae
Кустарничек с ползучим тонким корневищем и прямостоячими стеблями. Листья вечнозеленые. Цветки с бледно-розовым , колокольчатым венчиком собраны в поникшие кисти; в отличие от толокнянки околоцветник четырехчленный. Плод - красная сочная ягода. Цветет в апреле - мае.
Растение широко распространено по всей лесной зоне стран СНГ и Балтии.
Химический состав. Листья брусники содержат 6-9 % арбутина, гидрохинон, галловую и эллаговую кислоты, дубильные вещества (до 9 %), фла-воноиды, урсоловую кислоту.
Лекарственное сырье. Листья собирают в те же сроки, что и листья толокнянки. Они эллиптической формы, цельнокрайние, края немного завернуты к нижней стороне, голые, гладкие, темно-зеленые сверху; нижняя поверхность светло-зеленая, покрыта многочисленными бурыми или черными точками (вместилища). Запах отсутствует, вкус вяжущий, горьковатый.
Кроме цельных листьев, в аптеки поступают брикеты , полученные путем прессования крупного порошка листьев брусники. ГФ XI предусматривает цельное и измельченное сырье, в котором должно быть не менее 4,5 % арбутина.
Применение. Используют водные отвары в качестве мочегонного средства и при мочекаменной болезни.
Корневища мужского папоротника - Rhizomata Filicis maris
Растение. Мужской папоротник, или щитовник мужской, - Dryopteris filix mas (L.) Schott; семейство многоножковые - Polypodiaceae, иногда рассматривают как представителя семейства щитовниковых -Dryopteridaceae
Растение имеет два поколения - половое и бесполое. Бесполый диплоидный спорофит - многолетнее травянистое растение с зимующим корневищем. Корневище косорастущее, мощное, с многочисленными шнуровид-ными корнями. Верхний, растущий, конец корневища несет пучок крупных листьев длиной до 1 м, шириной 20-25 см. Нераспустившиеся листья улиткообразно свернуты. Черешок листа длиной до 25 см густо покрыт ржаво-бурыми чешуйками, в своем основании он очень сочен и расширен, при отмирании листа эта часть черешка остается на корневище. Пластинка листа темно-зеленая, в очертании продолговато-эллиптическая, двоякопе-ристорассеченная, сегменты 2-го порядка несут зубчики - они тупые, не игольчатые. На нижней поверхности листа развиваются бурые сорусы, закрытые почковидным покрывальцем, под которым находятся на длинных ножках овальные спорангии, содержащие бурые споры. Споры, прорастая, дают половое поколение - гаметофит в виде мелкого, зеленого, пластинчатого сердцевидного заростка, образующего архегонии и антеридии. После оплодотворения из зиготы вырастает бесполое поколение - спорофит, описанное выше растение.
Мужской папоротник растет в сырых тенистых лесах, под покровом ели или в елово-лиственных насаждениях - в европейской части России и Балтии; под покровом бука, граба и дуба - на Кавказе; под елью Шренка - на Тянь-Шане; под елью и пихтой - в сибирской тайге.
Химический состав.
О качестве корневища в первую очередь судят по содержанию "сырого филицина", понимая под ним сумму флороглюцидов. В состав сырого филицина входят бутирил-флороглюциды разной сложнос-ти строения. Наиболее простым соединением является аспидинол, содержащий одно флороглюциновое кольцо. Все остальные компоненты филицина являются ди- или тримерными флороглюцидами, в которых мономерами служат соединения , близкие к аспидинолу. Димером является альбаспидин, тримером - филиксовая кислота; чем больше колец, тем сильнее фармакологическое действие.
Корневища мужского папоротника, кроме флороглюцидов, содержат крахмал, сахарозу, дубильные вещества (7-8 %), жирное масло (до 6 %), летучие жирные кислоты и их эфиры (масляная кислота и др.).
Лекарственное сырье - корневища, покрытые многочисленными основаниями листовых черешков, с удаленной нижней (отмирающей) частью и без корней, длиной до 25 см, в самой толстой части до 7 см. Основания черешков листьев длиной 3-6 см, толщиной 6-11 мм, почти цилиндрической формы, расположены черепицеобразно косо вверх. На верхнем конце корневища находятся улиткообразно свернутые листовые почки. Основания черешков, особенно листовые почки, густо покрыты ржаво-бурыми пленчатыми чешуйками. Корневища и основания черешков снаружи темно-бурые, а на разрезе светло-зеленые. При этом на разрезе хорошо видны под лупой 6-9 центроксилемных проводящих пучков - "столбов", расположенных попериферии черешка неполным кольцом. Запах слабый, своеобразный. Вкус вначале сладковато-вяжущий, затем острый, тошнотворный.
Содержание сырого филицина в корневищах мужского папоротника зависит от разновидности папоротника 1 , района его заготовки, фазы вегетации. Заготавливают поздно летом и осенью. В это время корневища имеютнаибольшую сырьевую массу. Содержание сырого филицина должно быть не менее 1,8 % (ГФ X). Для медицинских целей пригодно сырье, сохранившее светло-зеленый цвет корневищ и черешков (в изломе). Срок хранения не более года в сухих, темных помещениях.
Примесями являются корневища женского папоротника и страусопера.
У женского папоротника (Athyrium filix femina Roth) корневище прямостоячее, листовые черешки снаружи почти черные, 3-гранной формы с двумя крупными проводящими пучками ("столбами"). У страусопера -Matteucia struthiopteris (L.) Todar - корневище прямостоячее, в черешках 2 крупных "столба".
Папоротники рода Dryopteris содержат в большем или меньшем количестве флороглюциды. После исследования некоторых из них, обладающих крупными корневищами, выяснилось, что наиболее перспективными оказались папоротник подальпийский (Dryorteris reados Fom.), папоротник шартрский, или игольчатый (Dryorteriscarthusiana (Vill.) H. P. Fuchs = D. spinulosa O. Kuntze), и папоротник расширенный, или австрийский (Dryorterisdilatata (HofFm.) A. Gray = D. austriaca (Jacq.) Woyn. ex Schinz et Thell.). Однако из-за обилия зарослей мужского папоротника в заготовке этих видов папоротника пока нет нужды.
Применение. Из корневищ мужского папоротника, свежесобранных и высушенных, приготавливают густой экстракт, получаемый путем экстракции эфиром. Препарат является эффективным противоглистным средством(ленточные черви). Список Б.
Фенологликозидами называется группа гликозидов, агликоном которых являются фенолы, оказывающие дезинфицирующее действие на дыхательные пути, почки и мочевые пути. Фенольные соединения содержат ароматические кольца с гидроксильной группой. Соединения, содержащие в ароматическом кольце больше одной гидроксильной группы, называются полифенолами. Они встречаются в различных частях многих растений - листьях, цветках (придают им окраску и аромат), плодах.
К группе фенолов с одним ароматическим кольцом относятся простые фенолы, фенолокислоты, фенолоспирты, оксикоричные кислоты. Фенологликозиды имеются в листьях толокнянки и брусники. Из фенолокислот часто встречается галловая кислота и значительно реже - салициловая (фиалка трехцветная). Фенолокислоты и их гликозиды содержатся в родиоле розовой.
Распространение.
В природе распространены довольно широко. Встречаются в семействах ивовых, брусничных, камнеломковых, толстянковых и др .
Физико-химические свойства.
Выделенные в чистом виде фенольные гликозиды - это белые кристаллические вещества, растворимые в воде, этаноле, нерастворимые в эфире и хлороформе. Отличаются оптической активностью, способны к гидролизу при нагревании с минеральными кислотами.Свободные фенолы и их гликозидные формы в индивидуальном состоянии представляют собой кристаллы белого или желтоватого цвета, растворимые в воде, этиловом и метиловом спиртах, этилацетате, а также в водных растворах щелочей и ацетата натрия. Все гликозиды оптически активны. Под действием минеральных кислот и ферментов фенологликозиды способны расщеплться на агликон и углевод.
Фенольные гликозиды, имеющие свободные гидроксилы дают характерные для фенольных соединений реакции: с железоаммонийными квасцами, с солями тяжелых металлов, с диазотированными ароматическими аминами (сульфаниловой кислотой или п-нитроанилином) и др.
Широко используют для обнаружения и идентификации фенологликозидов в растительном сырье хроматографию на бумаге и в тонком слое сорбента. При обработке специфическими реактивами и просвечивании в УФ-свете они проявляются в виде окрашенных пятен.
Для количественного определения фенолов наиболее часто применяют спектрофотометрический и фотоколориметрический методы, а иногда оксидиметрические методы. Например, для определения содержания арбутина в листья брусники и толокнянки по ГФ Х1 используется йодометрический метод, основанный на окислении гидрохинона, полученного после извлечения и гидролиза арбутина.
Способы получения.
Извлекаются из растительного сырья этанолом и метанолом.
Качественные реакции.
Фенольные гликозиды, со свободной гидроксильной группой дают все реакции, характерные для фенолов (реакция с железоаммониевыми квасцами, диазотирования и др.).
Применение.
Фенольные гликозиды, содержащие арбутин, обладают антимикробной и диуретической активностью. Гликозид солидрозин, содержащийся в коре ивы и подземных органах родиолы розовой, оказывает стимулирующее и адаптогенное действие. Фенологликозиды листьев толокнянки и брусники в организме расщепляются с выделением фенолов, обладающих противомикробным действием. А так как эти вещества образуются в почках, они дезинфицируют мочевые пути. Фенологликозиды родиолы розовой (золотого корня) снимают умственную и физическую усталость, а вещества трехцветной фиалки обладают отхаркивающим действием.
ЛЕКАРСТВЕННЫЕ РАСТЕНИЯ И СЫРЬЕ, СОДЕРЖАЩИЕ ФЕНОЛЬНЫЕ СОЕДИНЕНИЯ (общая характеристика).
1. Понятие о фенольных соединениях, распространение в растительном мире.
2. Роль фенольных соединений для жизнедеятельности растений.
3. Классификация фенольных соединений.
4. Биосинтез фенольных соединений.
Понятие о фенольных соединениях, распространение в растительном мире, роль фенольных соединений для жизнедеятельности растений.
Растения способны синтезировать и накапливать огромное количество соединений фенольной природы.
Фенолы – это ароматические соединения, содержащие в своей молекуле бензольное ядро с одной или несколькими гидроксильными группами.
Соединения, содержащие несколько ароматических колец, с одной или несколькими гидроксильными группами называются полифенолами .
Они встречаются в различных частях многих растений – в покровных тканях в плодах, проростках, листьях, цветках и
Придают им окраску и аромат пигменты фенольной природы - антоцианы;
большинство полифенолов –
Активные метаболиты клеточного обмена,
Играют важную роль в различных физиологических процессах, таких как, фотосинтез, дыхание, рост, устойчивость растений к инфекционным болезням, рост и репродукция;
Защищают растения от патогенных микроорганизмов и грибковых заболеваний.
Распространение.
Из фенолокислот часто встречается галловая кислота и значительно реже - салициловая (фиалка трехцветная). Фенолокислоты и их гликозиды содержатся в родиоле розовой.
К группе фенолов с одним ароматическим кольцом относятся простые фенолы, фенолокислоты, фенолоспирты, оксикоричные кислоты .
Фенологликозидами называется группа гликозидов, агликоном которых являются простые фенолы, оказывающие дезинфицирующее действие на дыхательные пути, почки и мочевые пути.
Фенологликозиды в природе распространены довольно широко. Встречаются в семействах ивовых, брусничных, камнеломковых, толстянковых и др., имеются в листьях толокнянки и брусники.
Природные фенолы часто проявляют высокую биологическую активность:
Препараты на основе фенольных соединений широко используются в качестве
Противомикробных, противовоспалительных, кровоостанавливающих, желчегонных, диуретических, гипотензивных, тонизирующих, вяжущих и слабительных средств.
Фенольные соединения имеют универсальное распространение в растительном мире. Они свойственны каждому растению и даже каждой растительной клетке. В настоящее время известно свыше двух тысяч природных фенольных соединений. На долю веществ этой группы приходится до 2-3% массы органического вещества растений, а в некоторых случаях - до 10% и более. Фенольные соединения обнаружены как в низших; грибах, мхах, лишайниках, водорослях, так и в высших споровых (папоротниках, хвощах) и цветковых растениях. У высших растений - в листьях, цветках, плодах, подземных органах.
Синтез фенольных соединений происходит только в растениях, животные потребляют фенольные соединения в готовом виде и могут их только преобразовывать
В растениях фенольные соединения играют важную роль.
1. Они являются обязательными участниками всех метаболических процессов: дыхания, фотосинтеза, гликолиза, фосфорилирования.
Исследованиями русского ученого биохимика В.И.Палладина (1912) установлено и подтверждено современными исследованиями, что фенольные соединения - «дыхательные хромогены»,т.е. ониучавствуют в процессе клеточного дыхания. Фенольные соединения выступают в качестве переносчиков водорода на конечных этапах процесса дыхания, азатем вновь окисляются специфическими ферментами оксидазами.
2. Фенольные соединения являются регуляторами роста, развития, и репродукции растений. При этом, оказывают как стимулирующее, так и ингибирующее (замедляющее) действие.
3. Фенольные соединения используются растениями как энергетический материал, выполняют структурную, опорную и защитную функции (повышает устойчивость растений к грибковым заболеваниям, обладают антибиотическим и противовирусным действием).
Классификация фенольных соединений.
В основе классификации природных фенольных соединений лежит биогенетический принцип. В соответствии с современными представлениями о биосинтезе и, исходя из структурных особенностей углеродного скелета, все фенолы можно разбить на 8 групп:
В зависимости от дополнительных атомов углерода они разделяются:
- - на соединения С 6 -ряда (без дополнительных атомов углерода);
- -соединения С 6 -Cj-ряда (один дополнительный атом углерода);
- - соединения С 6 -С 2 -ряда (два дополнительных атома углерода);
- - соединения С 6 -С 3 -ряда (три дополнительных атома углерода);
- - соединения С 6 -С 4 -ряда (четыре дополнительных атома углерода).
Соединения С (-ряда. К ним относятся простые фенолы. К этой группе веществ иногда относят и бензохиноны, хотя у них ароматическое кольцо почти всегда соединено с длинной изопреноид- ной цепочкой. Простые фенолы распространены не очень широко. Фенол в малых количествах обнаружен в хвое сосны, в составе эфирного масла смородины, табака и руты. Пирокатехин (7) найден в листьях тополя и эфедры, чешуе лука. Гваякол, монометило- вый эфир пирокатехина, в значительных количествах содержится в смоле бука [см.: 6, с. 108].
Соединения С 6 -С^ряда. К ним относятся производные окси- бензойной кислоты, которые часто называют фенольными кислотами, или фенолокислотами. Фенольные кислоты, особенно такие, как ванилиновая, я-гидроксибензойная (8), протокатеховая, галловая, обнаружены практически у всех исследованных покрытосеменных растений. Чаще они находятся в тканях в связанном состоянии и освобождаются при выделении и гидролизе. Например, салициловая кислота, которая находится в корнях дуба, выделяется в окружающую среду в качестве аллелопатического вещества.

Соединения С 6 -С 2 -ряда. К этому ряду соединений относятся фенолоспирты, фенилуксусные кислоты, ацетофенон. В отличие от фенольных кислот, они встречаются в растениях не так часто. В коре ивы присутствует салициловый спирт. Но особенно известен ванилин (ванильный альдегид), который содержится в плодах и ветвях ванильного дерева в виде гликозида.
Соединения С 6 -С^-ряда. Эту наиболее многочисленную и важную группу веществ часто называют также фенилпропано- идами. Она включает в себя оксикоричные кислоты (по международной номенклатуре их рекомендуется называть гидроксико- ричными кислотами), оксикоричные (гидроксикоричные) спирты, фенилпропены, а также кумарины, изокумарины и хромоны - соединения, у которых дополнительные атомы углерода замыкаются в конденсированное лактонное кольцо.
К гидроксикоричным кислотам относятся: л-гидроксикорич- ная, или л-кумаровая (9), кофейная, феруловая и синаповая. Как правило, в растениях они находятся в связанном состоянии (кроме кофейной). Для них характерна цис-транс- изомерия. Показано, что мис-изомеры гидроксикоричных кислот являются активаторами ростовых процессов [см.: 4, с. 157].

Помимо широко распространенной л-гидроксикоричной кислоты в некоторых растениях обнаружена о-гидроксикоричная кислота. Ее транс -форма устойчива, но гщс-форма (называемая кумариновой кислотой) в кислой среде циклизуется с образованием устойчивого лактона кумарина (10).

Кумарин - бесцветное кристаллическое вещество с приятным запахом, напоминающим запах сена [см.: 3, с. 319]. В растениях кумарин обычно содержится в виде гликозидов. При сенокосе растительные ткани повреждаются, и гликозиды из клеточного сока соприкасаются с ферментами цитоплазмы. После отщепления сахара кумаровая кислота после изомеризации замыкается в лактон - при этом вянущая трава приобретает запах сена.
Гидроксикоричные спирты являются производными соответствующих кислот. В ряде случаев фенилпропаноиды могут соединяться между собой и образовывать димеры, т. е. соединения типа (С 6 -С 3) 2 . Такие вещества называют лигнанами. Однако их обычно относят к группам димерных фенольных соединений.
Соединения С 6 -С 4 -ряда. К этому ряду соединений относятся нафтохиноны. Нафтохиноном является витамин К (филлохинон).