Основные изучаемые понятия:
Скорость химических реакций
Молярная концентрация
Кинетика
Гомогенные и гетерогенные реакции
Факторы, влияющие на скорость химических реакций
Катализатор, ингибитор
Катализ
Обратимые и необратимые реакции
Химическое равновесие
Химические реакции – это реакции, в результате которых из одних веществ получаются другие (из исходных веществ образуются новые вещества). Одни химические реакции протекают за доли секунды (взрыв), другие же – за минуты, дни, годы, десятилетия и т.д.
Например: мгновенно с воспламенением и взрывом происходит реакция горения пороха, а реакция потемнения серебра или ржавления железа (коррозия) идёт так медленно, что проследить за её результатом можно лишь по истечении длительного времени.
Для характеристики быстроты химической реакции используют понятие скорости химической реакции – υ.
Скорость химической реакции – это изменение концентрации одного из реагирующих веществ реакции в единицу времени.
Формула вычисления скорости химической реакции:
| υ = | с 2 – с 1 | = | ∆ с |
| t 2 – t 1 | ∆ t |
с 1 – молярная концентрация вещества в начальный момент времени t 1
с 2 – молярная концентрация вещества в начальный момент времени t 2
так как скорость химической реакции характеризуется изменением молярной концентрации реагирующих веществ (исходных веществ), то t 2 > t 1 , а с 2 > с 1 (концентрация исходных веществ убывает по мере протекания реакции).
Молярная концентрация (с) – это количество вещества в единице объёма. Единица измерения молярной концентрации - [моль/л].
Раздел химии, который изучает скорость химических реакций, называется химической кинетикой . Зная её законы, человек может управлять химическими процессами, задавать им определённую скорость.
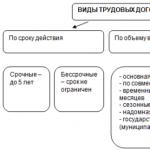
При расчёте скорости химической реакции необходимо помнить, что реакции делятся на гомогенные и гетерогенные.
Гомогенные реакции – реакции, которые протекают в одной среде (т.е. реагирующие вещества находятся в одинаковом агрегатном состоянии; например: газ + газ, жидкость + жидкость ).
Гетерогенные реакции – это реакции, протекающие между веществами в неоднородной среде (есть поверхность раздела фаз, т.е. реагирующие вещества находятся в разном агрегатном состоянии; например: газ + жидкость, жидкость + твёрдое вещество ).
Данная выше формула расчёта скорости химической реакции справедлива только для гомогенных реакций. Если реакция гетерогенная, то она может идти только на поверхности разделе реагирующих веществ.
Для гетерогенной реакции скорость вычисляется по формуле:
∆ν – изменение количества вещества
S – площадь поверхности раздела фаз
∆ t – промежуток времени, за который проходила реакция
Скорость химических реакций зависит от разных факторов: природы реагирующих веществ, концентрации веществ, температуры, катализаторов или ингибиторов.
Зависимость скорости реакций от природы реагирующих веществ.
Разберём данную зависимость скорости реакции на примере: опустим в две пробирки, в которых находится одинаковое количество раствора соляной кислоты (HCl), одинаковые по площади гранулы металлов: в первую пробирку гранулу железа (Fe), а во вторую – гранулу магния (Mg). В результате наблюдений, по скорости выделения водорода (Н 2), можно заметить, что с наибольшей скорость с соляной кислотой реагирует магний, чем железо . На скорость данной химической реакции оказывает влияние природа металла (т.е. магний более химически активный металл, чем железо, и поэтому он более энергично взаимодействует с кислотой).
Зависимость скорости химических реакций от концентрации реагирующих веществ.
Чем выше концентрация реагирующего (исходного) вещества, тем быстрее протекает реакция. И наоборот, чем меньше концентрация реагирующего вещества, тем медленнее идёт реакция.
Например: нальём в одну пробирку концентрированный раствор соляной кислоты (HCl), а в другую – разбавленный раствор соляной кислоты. Положим в обе пробирки по грануле цинка (Zn). Пронаблюдаем, по скорости выделения водорода, что реакция быстрее пойдёт в первой пробирке, т.к. концентрация соляной кислоты в ней больше, чем во второй пробирке.
Для определения зависимости скорости химической реакции применяют закон действия (действующих) масс : скорость химической реакции прямо пропорциональна произведению концентраций реагирующих веществ, взятых в степенях, которые равны их коэффициентам.
Например, для реакции, протекающей по схеме : nA + mB → D , скорость химической реакции определяют по формуле:
υ х.р. = k · C (A) n · C (B) m , где
υ х.р - скорость химической реакции
C (A) – А
C (В) – молярная концентрация вещества В
n и m – их коэффициенты
k – константа скорости химической реакции (справочная величина).
Закон действия масс не распространяется на вещества, находящиеся в твёрдом состоянии, т.к. их концентрация постоянна (вследствие того, что они реагируют лишь на поверхности, которая остаётся неизменной).
Например: для реакции 2 Cu + O 2 = 2CuO скорость реакции определяют по формуле:
υ х.р. = k · C(O 2)
ЗАДАЧА: Константа скорости реакции 2А + В = D равна 0,005. вычислить скорость реакции при молярной концентрации вещества А = 0,6 моль/л, вещества В = 0,8 моль/л.
Зависимость скорости химической реакции от температуры .
Эта зависимость определяется правилом Вант – Гоффа (1884г.): при увеличении температура на каждые 10 С о скорость химической реакции увеличивается в среднем в 2 – 4 раза.
Так, взаимодействие водорода (Н 2) и кислорода (О 2) при комнатной температуре почти не происходит, так мала скорость этой химической реакции. Но при температуре 500 С о эта реакция протекает за 50 минут, а при температуре 700 С о – почти мгновенно.
Формула расчёта скорости химической реакции по правилу Вант – Гоффа:
где: υ t 1 и υ t 2 - скорости химических реакций при t 2 и t 1
γ – температурный коэффициент, который показывает во сколько раз увеличивается скорость реакции с повышением температуры на 10 С о.
Изменение скорости реакции:
2. Подставим данные из условия задачи в формулу:
Зависимость скорости реакций от специальных веществ – катализаторов и ингибиторов.
Катализатор – вещество, которое увеличивает скорость химической реакции, но само в ней не участвует.
Ингибитор – вещество, замедляющее химическую реакцию, но само в ней не участвующие.
Пример: в пробирку с раствором 3% перекиси водорода (Н 2 О 2), которую нагрели, внесём тлеющую лучину – она не загорится, т.к. скорость реакции разложения перекиси водорода на воду (Н 2 О) и кислород (О 2) очень мала, и образовавшегося кислорода недостаточно для проведения качественной реакции на кислород (поддержание горения). Теперь внесём в пробирку немного чёрного порошка оксида марганца (IV) (MnO 2) и увидим, что началось бурное выделение пузырьков газа (кислорода), а внесённая в пробирку тлеющая лучина ярко вспыхивает. MnO 2 – катализатор данной реакции, он ускорил скорость реакции, но сам в ней не участвовал (это можно доказать взвесив катализатор до и после проведения реакции – его масса не изменится).
В жизни мы сталкиваемся с разными химическими реакциями. Одни из них, как ржавление железа, могут идти несколько лет. Другие, например, сбраживание сахара в спирт, - несколько недель. Дрова в печи сгорают за пару часов, а бензин в моторе - за долю секунды.
Чтобы уменьшить затраты на оборудование, на химических заводах повышают скорость реакций. А некоторые процессы, например, порчу пищевых продуктов, коррозию металлов, - нужно замедлить.
Скорость химической реакции можно выразить как изменение количества вещества (n, по модулю) в единицу времени (t) - сравните скорость движущегося тела в физике как изменение координат в единицу времени: υ = Δx/Δt . Чтобы скорость не зависела от объема сосуда, в котором протекает реакция, делим выражение на объем реагирующих веществ (v), т. е. получаем изменение количества вещества в единицу времени в единице объема, или изменение концентрации одного из веществ в единицу времени :
n 2 − n 1 Δn
υ = –––––––––– = –––––––– = Δс/Δt (1)
(t 2 − t 1) v Δt v
где c = n / v - концентрация вещества,
Δ (читается «дельта») - общепринятое обозначение изменения величины.
Если в уравнении у веществ разные коэффициенты, скорость реакции для каждого из них, рассчитанная по этой формуле будет различной. Например, 2 моль серни́стого газа прореагировали полностью с 1 моль кислорода за 10 секунд в 1 литре:
2SO 2 + O 2 = 2SO 3
Скорость по кислороду будет: υ = 1: (10 1) = 0,1 моль/л·с
Скорость по серни́стому газу: υ = 2: (10 1) = 0,2 моль/л·с - это не нужно запоминать и говорить на экзамене, пример приведен для того, чтобы не путаться, если возникнет этот вопрос.
Скорость гетерогенных реакций (с участием твердых веществ) часто выражают на единицу площади соприкасающихся поверхностей:
Δn
υ = –––––– (2)
Δt S
Гетерогенными называются реакции, когда реагирующие вещества находятся в разных фазах:
- твердое вещество с другим твердым, жидкостью или газом,
- две несмешивающиеся жидкости,
- жидкость с газом.
Гомогенные реакции протекают между веществами в одной фазе:
- между хорошо смешивающимися жидкостями,
- газами,
- веществами в растворах.
Условия, влияющие на скорость химических реакций
1) Скорость реакции зависит от природы реагирующих веществ . Проще говоря, разные вещества реагируют с разной скоростью. Например, цинк бурно реагирует с соляной кислотой, а железо довольно медленно.
2) Скорость реакции тем больше, чем выше концентрация веществ. С сильно разбавленной кислотой цинк будет реагировать значительно дольше.
3) Скорость реакции значительно повышается с повышением температуры . Например, для горения топлива необходимо его поджечь, т. е. повысить температуру. Для многих реакций повышение температуры на 10° C сопровождается увеличением скорости в 2–4 раза.
4) Скорость гетерогенных реакций увеличивается с увеличением поверхности реагирующих веществ . Твердые вещества для этого обычно измельчают. Например, чтобы порошки железа и серы при нагревании вступили в реакцию, железо должно быть в виде мелких опилок.
Обратите внимание, что в данном случае подразумевается формула (1) ! Формула (2) выражает скорость на единице площади, следовательно не может зависеть от площади.
5) Скорость реакции зависит от наличия катализаторов или ингибиторов.
Катализаторы - вещества, ускоряющие химические реакции, но сами при этом не расходующиеся. Пример - бурное разложение перекиси водорода при добавлении катализатора - оксида марганца (IV):
2H 2 O 2 = 2H 2 O + O 2
Оксид марганца (IV) остается на дне, его можно использовать повторно.
Ингибиторы - вещества, замедляющие реакцию. Например, для продления срока службы труб и батарей в систему водяного отопления добавляют ингибиторы коррозии. В автомобилях ингибиторы коррозии добавляются в тормозную, охлаждающую жидкость.
Еще несколько примеров.
Мы постоянно сталкиваемся с различными химическими взаимодействиями. Сгорание природного газа, ржавление железа, скисание молока - далеко не все процессы, которые подробно изучаются в школьном курсе химии.
Для протекания одних реакций требуются доли секунд, а для некоторых взаимодействий нужны дни и недели.
Попробуем выявить зависимость скорости реакции от температуры, концентрации, иных факторов. В новом образовательном стандарте на данный вопрос отводится минимальное количество учебного времени. В тестах единого государственного экзамена есть задания на зависимость скорости реакции от температуры, концентрации и даже предлагаются расчетные задачи. Многие старшеклассники испытывают определенные сложности с поиском ответов на эти вопросы, поэтому подробно проанализируем данную тему.
Актуальность рассматриваемого вопроса
Информация о скорости реакции имеет важное практическое и научное значение. К примеру, в конкретном производстве веществ и продуктов от данной величины напрямую зависит производительность аппаратуры, стоимость товаров.
Классификация протекающих реакций
Существует прямая зависимость между агрегатным состоянием исходных компонентов и продуктов, образующихся в ходе гетерогенные взаимодействия.
Под системой принято подразумевать в химии вещество либо их совокупность.
Гомогенной считают такую систему, которая состоит из одной фазы (одинакового агрегатного состояния). В качестве ее примера можно упомянуть смесь газов, несколько различных жидкостей.
Гетерогенной является система, в которой реагирующие вещества находятся в виде газов и жидкостей, твердых тел и газов.
Существует не только зависимость скорости реакции от температуры, но и от того, в какой фазе используются компоненты, вступающие в анализируемое взаимодействие.
Для однородного состава характерно протекание процесса по всему объему, что существенно повышает его качество.
Если исходные вещества находятся в разных фазовых состояниях, в таком случае максимальное взаимодействие наблюдается на границе раздела фаз. К примеру, при растворении активного металла в кислоте, образование продукта (соли) наблюдается только на поверхности их соприкосновения.

Математическая зависимость между скоростью процесса и различными факторами
Как выглядит уравнение зависимости скорости химической реакции от температуры? Для гомогенного процесса скорость определяется количеством вещества, которое вступает во взаимодействие либо образуется в ходе реакции в объеме системы за единицу времени.
Для гетерогенного процесса скорость определяется через количество вещества, реагирующего либо получаемого в процессе на единице площади за минимальный промежуток времени.

Факторы, влияющие на скорость химической реакции
Природа реагирующих веществ - одна из причин разной скорости протекания процессов. Например, щелочные металлы при комнатной температуре образуют с водой щелочи, причем процесс сопровождается интенсивным выделением газообразного водорода. Благородные металлы (золото, платина, серебро) не способны к подобным процессам ни при комнатной температуре, ни при нагревании.
Природа реагирующих веществ - тот фактор, который учитывают в химической промышленности, чтобы повысить рентабельность производства.
Выявлена зависимость между концентрацией реагентов и быстротой протекания химической реакции. Чем она будет выше, тем больше частиц будет сталкиваться, следовательно, процесс будет протекать быстрее.
Закон действующих масс в математическом виде описывает прямо пропорциональную зависимость между концентрацией исходных веществ и быстротой протекания процесса.
Он был сформулирован в середине девятнадцатого века русским химиком Н. Н. Бекетовым. Для каждого процесса определяется константа реакции, которая не связана ни с температурой, ни с концентрацией, ни с природой реагирующих веществ.
Для того чтобы ускорить реакцию, в которой участвует твердое вещество, нужно измельчить его до порошкообразного состояния.
При этом происходит возрастание площади поверхности, что позитивно сказывается на быстроте протекания процесса. Для дизельного топлива применяют специальную систему впрыска, благодаря чему при соприкосновении ее с воздухом скорость процесса сгорания смеси углеводородов существенно возрастает.

Нагревание
Зависимость скорости химической реакции от температуры объясняется молекулярно-кинетической теорией. Она позволяет провести расчет количества соударений между молекулами реагентов при определенных условиях. Если вооружиться подобной информацией, то при обычных условиях все процессы должны протекать мгновенно.
Но если рассмотреть конкретный пример зависимости скорости реакции от температуры, оказывается, что для взаимодействия необходимо сначала разорвать химические связи между атомами, чтобы из них образовались новые вещества. Это требует существенных затрат энергии. Какова зависимость скорости реакции от температуры? Энергия активации определяет возможность разрыва молекул, именно она характеризует реальность процессов. Ее единицами измерения является кДж/моль.
При недостаточном показателе энергии столкновение будет малоэффективным, поэтому оно не сопровождается образованием новой молекулы.

Графическое представление
Зависимость скорости химической реакции от температуры можно представить графически. При нагревании число столкновений между частицами возрастает, что способствует ускорению взаимодействия.
Как выглядит график зависимости скорости реакции от температуры? По горизонтали откладывается энергия молекул, а по вертикали указывается число частиц, имеющих высокий энергетический запас. Графиком является кривая, по которой можно судить о скорости протекания конкретного взаимодействия.
Чем больше будет отличие энергии от среднего показателя, тем дальше располагается от максимума точка кривой, и меньший процент молекул имеет такой запас энергии.

Важные аспекты
Можно ли записать уравнение зависимости константы скорости реакции от температуры? Ее повышение отражается на увеличении скорости процесса. Такая зависимость характеризуется определенной величиной, называемой температурным коэффициентом скорости процесса.
Для любого взаимодействия выявлена зависимость константы скорости реакции от температуры. В случае ее повышения на 10 градусов происходит увеличение скорости процесса в 2-4 раза.
Зависимость скорости гомогенных реакций от температуры можно представить в математическом виде.
Для большинства взаимодействий при комнатной температуре коэффициент находится в диапазоне от 2 до 4. К примеру, при значении температурного коэффициента 2,9 рост температуры на 100 градусов ускоряет процесс почти в 50000 раз.
Зависимость скорости реакции от температуры легко можно объяснить разной величиной энергии активации. Минимальную величину она имеет при проведении ионных процессов, которые определяются только взаимодействием катионов и анионов. Многочисленные эксперименты свидетельствуют о мгновенном протекании подобных реакций.
При высоком значении энергии активации лишь незначительное количество столкновений между частицами будет приводить к осуществлению взаимодействия. При среднем значении энергии активации, реагенты будут взаимодействовать со средней скоростью.
Задания на зависимость скорости реакции от концентрации и температуры рассматриваются только на старшей ступени обучения, часто вызывают у ребят серьезные затруднения.
Измерение быстроты протекания процесса
Те процессы, которые нуждаются в существенной энергии активации, предполагают первоначальный разрыв либо ослабление связей между атомами в исходных веществах. При этом происходит их переход в некое промежуточное состояние, именуемое активированным комплексом. Он является неустойчивым состоянием, довольно быстро распадается на продукты реакции, процесс сопровождается выделением дополнительной энергии.
В простейшем варианте активированный комплекс является конфигурацией атомов с ослабленными старыми связями.

Ингибиторы и катализаторы
Проанализируем зависимость скорости ферментативной реакции от температуры среды. Такие вещества осуществляют функцию ускорителей процесса.
Сами они не являются участниками взаимодействия, их количество после завершения процесса остается без изменений. Если катализаторы способствуют увеличению скорости реакции, то ингибиторы, напротив, замедляют этот процесс.
Суть этого заключается в образовании промежуточных соединений, в результате чего и наблюдается изменение быстроты протекания процесса.
Заключение
В мире ежеминутно происходят разнообразные химические взаимодействия. Как установить зависимость скорости реакции от температуры? Уравнение Аррениуса является математическим объяснением связи константы скорости и температуры. Оно дает представление о тех значениях энергии активации, при которых возможно разрушение либо ослабление связей между атомами в молекулах, распределение частиц в новые химические вещества.
Благодаря молекулярно-кинетической теории можно предсказывать вероятность протекания взаимодействий между исходными компонентами, рассчитывать скорость протекания процесса. Среди тех факторов, которые оказывают воздействие на скорость реакции, особое значение имеет изменение температурного показателя, процентной концентрации взаимодействующих веществ, площадь поверхности соприкосновения, присутствие катализатора (ингибитора), а также природа взаимодействующих компонентов.
7.1. Гомогенные и гетерогенные реакции
Химические вещества могут находиться в разных агрегатных состояниях, при этом их химические свойства в разных состояниях одинаковы, однако активность отличается (что на прошлой лекции было показано на примере теплового эффекта химической реакции).
Рассмотрим различные комбинации агрегатных состояний, в которых могут находиться два вещества А и Б.
A (г.), Б (г.) |
||||||||||||||||||||||||||||||
A (тв.), Б (тв.) | A (ж.), Б (тв.) | смешиваются | A(тв.), Б (г.) | A (ж.), Б (г.) |
||||||||||||||||||||||||||
смешиваются | (раствор) | |||||||||||||||||||||||||||||
гетерогенная | гетерогенная | гетерогенная | гомогенная | гетерогенная | гетерогенная | гомогенная |
||||||||||||||||||||||||
Hg(ж.) + HNO3 | H2 O + D2 O | Fe + O2 | H2 S + H2 SO4 | CO + O2 |
||||||||||||||||||||||||||
Фазой называется область химической системы, в пределах которой все свойства системы постоянны (одинаковы) или непрерывно меняются от точки к точке. Отдельными фазами являются каждое из твердых веществ, кроме того существуют фазы раствора и газа.
Гомогенной называетсяхимическая система , в которой все вещества находятся в одной фазе (в растворе или в газе). Если фаз несколько, то система называется
гетерогенной.
Соответственно химическая реакция называетсягомогенной , еслиреагенты находятся в одной фазе. Еслиреагенты находятся в разных фазах, тохимическая реакция называетсягетерогенной .
Нетрудно понять, что поскольку для возникновения химической реакции требуется контакт реагентов, то гомогенная реакция происходит одновременно во всем объеме раствора или реакционного сосуда, тогда как гетерогенная реакция происходит на узкой границе между фазами - на поверхности раздела фаз. Таким образом, чисто теоретически гомогенная реакция происходит быстрее, чем гетерогенная.
Таким образом, мы переходим к понятию скорость химической реакции .
Скорость химической реакции. Закон действующих масс. Химическое равновесие.
7.2. Скорость химической реакции
Раздел химии, который изучает скорости и механизмы химических реакций является разделом физической химии и называется химической кинетикой .
Скоростью химической реакции называется изменение количества вещества в единицу времени в единице объема реагирующей системы (для гомогенной реакции) или на единице площади поверхности (для гетерогенной реакции).
Таким образом, если объем | или площадь | поверхности раздела фаз |
|||||||||
не изменяются, то выражения для скоростей химических реакций имеют вид: |
|||||||||||
hom o | |||||||||||
Отношение изменения количества вещества к объему системы можно интерпретировать как изменение концентрации данного вещества.
Отметим, что для реагентов в записи выражения для скорости химической реакции ставят знак «минус», так как концентрация реагентов уменьшается, а скорость химической реакции – вообще-то величина положительная.
Дальнейшие умозаключения базируются на простых физических соображениях, которые рассматривают химическую реакцию как следствие взаимодействия нескольких частиц.
Элементарной (или простой) называют химическую реакцию, происходящую в одну стадию. Если стадий несколько, то подобные реакции называют сложными, или составными, или брутто-реакциями.
В 1867 году для описания скорости химической реакции был предложен закон действующих масс : скорость элементарной химической реакции пропорциональная концентрациям реагирующих веществ в степенях стехиометрических коэффициентов.n A +m B P,
A, B – реагенты, P – продукты, n ,m – коэффициенты.
W =k n m
Коэффициент k называется константой скорости химической реакции,
характеризует природу взаимодействующих частиц и не зависит от концентрации частиц.
Скорость химической реакции. Закон действующих масс. Химическое равновесие. Величины n иm называютсяпорядком реакции по веществу А и B соответственно, а
их сумма (n +m ) –порядком реакции .
Для элементарных реакций порядок реакции может быть 1, 2 и 3.
Элементарные реакции с порядком 1 называют мономолекулярными, с порядком 2 – бимолекулярными, с порядком 3 – тримолекулярными по числу участвующих молекул. Элементарных реакций выше третьего порядка неизвестно – расчеты показывают, что одновременная встреча четырех молекул в одной точке слишком невероятное событие.
Поскольку сложная реакция состоит из некоторой последовательности элементарных реакций, то её скорость может быть выражена через скорости отдельных стадий реакции. Поэтому для сложных реакций порядок может быть любым , в том числе, дробным или нулевым (нулевой порядок реакции говорит о том, что реакция происходит с постоянной скоростью и не зависит от концентрации реагирующих частицW =k ).
Самую медленную из стадий сложного процесса обычно называют лимитирующей стадией (скоростьлимитирующей стадией).
Представьте себе, что большое количество молекул пошли в бесплатный кинотеатр, но на входе стоит контролер, который проверяет возраст каждой молекулы. Поэтому в двери кинотеатра заходит поток вещества, а в кинозал молекулы проникают по одной, т.е. очень медленно.
Примерами элементарных реакций первого порядка являются процессы термического или радиоактивного распада, соответственно константа скорости k характеризует либо вероятность разрыва химической связи, либо вероятность распада в единицу времени.
Примеров элементарных реакций второго порядка очень много – это наиболее привычный нам способ течения реакций – частица А налетела на частицу B, произошло какое-то превращение и что-то там получилось (обратите внимание, что продукты в теории ни на что не влияют – все внимание уделяется только реагирующим частицам).
Напротив, элементарных реакций третьего порядка довольно мало, так как трём частицам одновременно встретиться удается довольно редко.
В качестве иллюстрации посмотрим предсказательную силу химической кинетики.
Скорость химической реакции. Закон действующих масс. Химическое равновесие.
Кинетическое уравнение первого порядка
(иллюстративный дополнительный материал)
Рассмотрим гомогенную реакцию первого порядка, константа скорости которой равна k , начальная концентрация вещества A равна [A]0 .
По определению скорость гомогенной химической реакции равна |
||||||||||||||||||
K [ A ] | изменению концентрации в единицу времени. Раз вещество A – |
|||||||||||||||||
реагент, ставим знак «минус». | ||||||||||||||||||
Такое уравнение называется дифференциальным (есть |
||||||||||||||||||
производная) | ||||||||||||||||||
[ A ] | Для его решения в левую часть переносим величины |
|||||||||||||||||
концентраций, а в правую – времени. | ||||||||||||||||||
Если равны производные двух функций, то сами функции |
||||||||||||||||||
должны отличаться не более, чем на константу. | ||||||||||||||||||
Для решения данного уравнения берут интеграл левой части (по |
||||||||||||||||||
концентрации) и правой части (по времени). Чтобы не пугать |
||||||||||||||||||
ln[ A ] = −kt +C | слушателей, ограничимся ответом. | |||||||||||||||||
Значок ln – натуральный логарифм, т.е. число b, такое что | ||||||||||||||||||
= [ A ] ,e = 2,71828… | ||||||||||||||||||
ln[ A ]- ln0 = - kt | Константу C находят из начальных условий: | |||||||||||||||||
при t = 0 начальная концентрация равна [A]0 | ||||||||||||||||||
[ A ] | Раз логарифм – | это степень числа, используем свойства степеней |
||||||||||||||||
[ A ]0 | e a− b= | |||||||||||||||||
Теперь избавимся от противного логарифма (см. определение |
||||||||||||||||||
логарифма на 6-7 строчек выше), | для чего возведем число | |||||||||||||||||
в степень левой части уравнения и правой части уравнения. | ||||||||||||||||||
[ A ] | E − kt | Умножим на [A]0 | ||||||||||||||||
[ A ]0 | ||||||||||||||||||
Кинетическое уравнение первого порядка. | ||||||||||||||||||
[ A ]= 0 × e − kt | На основании | полученного кинетического уравнения первого |
||||||||||||||||
порядка может | рассчитана | концентрация вещества | ||||||||||||||||
в любой момент времени | ||||||||||||||||||
Для целей нашего курса данный вывод носит ознакомительный характер, для того чтобы продемонстрировать Вам применение математического аппарата для расчета хода химической реакции. Следовательно, грамотный химик не может не знать математику. Учите математику!

Скорость химической реакции. Закон действующих масс. Химическое равновесие. График зависимости концентрации реагентов и продуктов от времени может быть качественно изображен следующим образом (на примере необратимой реакции первого порядка)
Факторы, которые влияют на скорость реакции
1. Природа реагирующих веществ
Например, скорость реакции следующих веществ: H2 SO4 , CH3 COOH, H2 S, CH3 OH – с гидроксид-ионом будет различаться в зависимости от прочности связи H-O. Для оценки прочности данной связи можно использовать величину относительного положительного заряда на атоме водорода: чем больше заряд, тем легче будет идти реакция.
2. Температура
Жизненный опыт подсказывает нам, что скорость реакции от температуры зависит и увеличивается с ростом температуры. Например, процесс скисания молока быстрее происходит при комнатной температуре, а не в холодильнике.
Обратимся к математическому выражению закона действующих масс.
W =k n m
Раз левая часть этого выражения (скорость реакции) от температуры зависит, следовательно, правая часть выражения также зависит от температуры. При этом концентрация, разумеется, от температуры не зависит: например, молоко сохраняет свою жирность 2,5% и в холодильнике, и при комнатной температуре. Тогда, как говаривал Шерлок Холмс оставшееся решение и есть верное, каким бы странным оно ни казалось: от температуры зависит константа скорости!

Скорость химической реакции. Закон действующих масс. Химическое равновесие. Зависимость константы скорости реакции от температуры выражается посредством уравнения Аррениуса:
− E a
k = k0 eRT ,
в котором
R = 8,314 Дж·моль-1 ·К-1 – универсальная газовая постоянная,
E a – энергия активации реакции (см. ниже), её условно считают не зависящей от температуры;
k 0 – предэкспоненциальный множитель (т.е. множитель, который стоит перед экспонентойe ), величина которого тоже почти не зависит от температуры и определяется, в первую очередь, порядком реакции.
Так, величина k0 составляет примерно для реакции первого порядка 1013 с-1 , для реакции второго порядка – 10 -10 л·моль-1 ·с-1 ,
для реакции третьего порядка – 10 -33 л2 ·моль-2 ·с-1 . Эти значения запоминать не обязательно.
Точные значения k0 для каждой реакции определяют экспериментально.
Понятие энергии активации становится ясным из следующего рисунка. Фактически энергия активации представляет собой энергию, которой должна обладать реагирующая частица, для того, чтобы реакция произошла.
При этом если мы нагреваем систему, то энергия частиц повышается (пунктирный график), тогда как переходное состояние (≠) остается на прежнем уровне. Разница в энергии между переходным состоянием и реагентами (энергия активации) сокращается, а скорость реакции согласно уравнению Аррениуса возрастает.
Скорость химической реакции. Закон действующих масс. Химическое равновесие. Кроме уравнения Аррениуса, существует уравнение Вант-Гоффа, которое
характеризует зависимость скорости реакции от температуры посредством температурного коэффициента γ:
Температурный коэффициент γ показывает, во сколько раз вырастет скорость химической реакции при изменении температуры на 10o .
Уравнение Вант-Гоффа:
T 2− T 1
W (T 2 )= W (T 1 )× γ10
Обычно коэффициент γ находится в диапазоне от 2 до 4. По этой причине химики часто пользуются приближением, что увеличение температуры на 20o приводит к возрастанию скорости реакции на порядок (т.е. в 10 раз).
Скорость химической реакции зависит от следующих факторов:
1) Природа реагирующих веществ.
2) Поверхность соприкосновения реагентов.
3) Концентрация реагирующих веществ.
4) Температура.
5) Присутствие катализаторов.
Скорость гетерогенных реакций зависит также от:
а) величины поверхности раздела фаз (с увеличением поверхности раздела фаз скорость гетерогенных реакций увеличивается);
б) скорости подвода реагирующих веществ к поверхности раздела фаз и скорости отвода от нее продуктов реакции.
Факторы, влияющие на скорость химической реакции:
1. Природа реагентов. Большую роль играет характер химических связей в соединениях, строение их молекул. Например, выделение водорода цинком из раствора хлороводородной кислоты происходит значительно быстрее, чем из раствора уксусной кислоты, так как полярность связи Н-С1 больше, чем связи О-Н в молекуле СН 3 СООН, иначе говоря, из-за того, что НСl - сильный электролит, а СН 3 СООН - слабый электролит в водном растворе.
2. Поверхность соприкосновения реагентов. Чем больше поверхность соприкосновения реагирующих веществ, тем быстрее протекает реакция. Поверхность твердых веществ может быть увеличена путем их измельчения, а для растворимых веществ - путем их растворения. Реакции в растворах протекают практически мгновенно.
3. Концентрация реагентов. Чтобы произошло взаимодействие, частицы реагирующих веществ в гомогенной системе должны столкнуться. При увеличении концентрации реагирующих веществ скорость реакций увеличивается. Это объясняется тем, что при увеличении количества вещества в единице объема увеличивается число столкновений между частицами реагирующих веществ. Число столкновений пропорционально числу частиц реагирующих веществ в объеме реактора, т. е. их молярным концентрациям.
Количественно зависимость скорости реакции от концентрации реагирующих веществ выражается законом действующих масс (Гульдберг и Вааге, Норвегия, 1867 г.): скорость химической реакции пропорциональна произведению концентраций реагирующих веществ.
Для реакции:
aA + bB ↔ cC + dD
скорость реакции в соответствии с законом действующих масс равна:
υ = k· [A ] υ a · [B ] υ b , (9)
где [А] и [В] - концентрации исходных веществ;
k - константа скорости реакции , которая равна скорости реакции при концентрациях реагирующих веществ [А] = [В] = 1 моль/л.
Константа скорости реакции зависит от природы реагирующих веществ, температуры, но не зависит от концентрации веществ.
Выражение (9) называется кинетическим уравнением реакции. В кинетические уравнения входят концентрации газообразных и растворенных веществ, но не входят концентрации твердых веществ:
2SO 2(г) + O 2(г) = 2SO 3(г) ; υ = k· 2 · [О 2 ];
СuО (тв.) + Н 2(г) = Сu (тв) + Н 2 О (г) ; υ = k· .
По кинетическим уравнениям можно рассчитывать, как изменяется скорость реакции при изменении концентрации реагирующих веществ.
Влияние катализатора.
5. Температура реакции. Теория активных соударений
Для того чтобы совершился элементарный акт химического взаимодействия, реагирующие частицы должны столкнуться друг с другом. Однако не каждое столкновение приводит к химическому взаимодействию. Химическое взаимодействие происходит в том случае, когда частицы приближаются на расстояния, при которых возможно перераспределение электронной плотности и возникновение новых химических связей. Взаимодействующие частицы должны обладать энергией, достаточной для преодоления сил отталкивания, возникающих между их электронными оболочками.
Переходное состояние - состояние системы, при котором уравновешены разрушение и создание связи. В переходном состоянии система находится в течение небольшого (10 -15 с) времени. Энергия, которую необходимо затратить, чтобы привести систему в переходное состояние, называется энергией активации. В многоступенчатых реакциях, которые включают в себя несколько переходных состояний, энергия активации соответствует наибольшему значению энергии. После преодоления переходного состояния молекулы вновь разлетаются с разрушением старых связей и образованием новых или с преобразованием исходных связей. Оба варианта возможны, так как происходят с высвобождением энергии. Существуют вещества, способные уменьшить энергию активации для данной реакции.
Активные молекулы А 2 и В 2 при столкновении объединяются в промежуточный активный комплекс А 2 ...В 2 с ослаблением, а затем и разрывом связей А-А и В-В и упрочнением связей А-В.
«Энергия активации» реакции образования НI (168 кДж/моль) значительно меньше, чем энергия, необходимая для полного разрыва связи в исходных молекулах Н 2 и I 2 (571 кДж/моль). Поэтому путь реакции через образование активного (активированного} комплекса энергетически более выгоден, чем путь через полный разрыв связей в исходных молекулах. Через образование промежуточных активных комплексов происходит подавляющее большинство реакций. Положения теории активного комплекса разработаны Г. Эйрингом и М. Поляни в 30 годах XX в.
Энергия активации представляет собой избыток кинетической энергии частиц относительно средней энергии, необходимой для химического превращения сталкивающихся частиц. Реакции характеризуются различными величинами энергии активации (Е а). В большинстве случаев энергия активации химических реакций между нейтральными молекулами составляет от 80 до 240 кДж/моль. Для биохимических процессов значения Е а зачастую ниже - до 20 кДж/моль. Это объясняйся тем, что абсолютное большинство биохимических процессов протекает через стадию фермент-субстратных комплексов. Энергетические барьеры ограничивают протекание реакции. Благодаря этому в принципе возможные реакции (при Q < 0) практически всегда не протекают или замедляются. Реакции с энергией активации выше 120 кДж/моль настолько медленны, что их протекание трудно заметить.
Для осуществления реакции молекулы при столкновении должны быть определенным образом ориентированы и обладать достаточной энергией. Вероятность надлежащей ориентации при столкновении характеризуют с помощью энтропии активации ∆S a . Перераспределению электронной плотности в активном комплексе благоприятствует условие, когда при столкновении молекулы А 2 и В 2 ориентированы, как это показано на рис. 3а, тогда как при ориентации, показанной на рис. 3б, вероятность реакции еще гораздо меньше - на рис. 3в.

Рис. 3. Благоприятная (а) и неблагоприятные (б, в) ориентации молекул А 2 и В 2 при столкновении
Уравнение, характеризующее зависимость скорости и реакции от температуры, энергии активации и энтропии активации, имеет вид:
![]() (10)
(10)
где k - константа скорости реакции;
А - в первом приближении общее число столкновений между молекулами за единицу времени (секунду) в единице объема;
е - основание натуральных логарифмов;
R - универсальная газовая постоянная;
Т - абсолютная температура;
Е а - энергия активации;
∆S a - изменение энтропии активации.
Уравнение (11) выведено Аррениусом в 1889 году. Предэкспоненциальный множитель А пропорционален общему числу соударений между молекулами в единицу времени. Его размерность совпадает с размерностью константы скорости и зависит от суммарного порядка реакции.
Экспонента равна доле активных соударений от их общего числа, т.е. столкнувшиеся молекулы должны иметь достаточную энергию взаимодействия. Вероятность же их нужной ориентации в момент соударения пропорциональна .
При обсуждении закона действующих масс для скорости (9) специально было оговорено, что константа скорости есть постоянная величина, не зависящая от концентраций реагентов. При этом предполагалось, что все химические превращения протекают при постоянной температуре. Вместе с тем, быстрота химического превращения может существенно изменяться при понижении или повышении температуры. С точки зрения закона действующих масс это изменение скорости обусловлено температурной зависимостью константы скорости, так как концентрации реагирующих веществ лишь незначительно меняются вследствие теплового расширения или сжатия жидкости.
Наиболее хорошо известным фактом является возрастание скорости реакций с увеличением температуры. Такой тип температурной зависимости скорости называется нормальным (рис. 3 а). Этот тип зависимости характерен для всех простых реакций.

Рис. 3. Типы температурной зависимости скорости химических реакций: а - нормальная;
б - аномальная; в - ферментативная
Однако в настоящее время хорошо известны химические превращения, скорость которых падает с увеличением температуры, такой тип температурной зависимости скорости называется аномальным . В качестве примера можно привести газофазную реакцию азота (II) оксида с бромом (рис. 3 б).
Особый интерес для медиков представляет зависимость от температуры скорости ферментативных реакций, т.е. реакций с участием ферментов. Практически все реакции, протекающие в организме, относятся к этому классу. Например, при разложении пероксида водорода в присутствии фермента каталазы скорость разложения зависит от температуры. В интервале 273-320 К температурная зависимость имеет нормальный характер. С увеличением температуры скорость возрастает, с уменьшением - падает. При подъеме температуры выше 320 К наблюдается резкое аномальное падение скорости разложения пероксида. Сходная картина имеет место и для других ферментативных реакций (рис. 3 в).
Из уравнения Аррениуса для k видно, что, поскольку Т входит в показатель степени, скорость химической реакции очень чувствительна к изменению температуры. Зависимость скорости гомогенной реакции от температуры может быть выражена правилом Вант-Гоффа, согласно которому при увеличении температуры на каждые 10° скорость реакции возрастает в 2-4 раза; число, показывающее во сколько раз возрастает скорость данной реакции при повышении температуры на 10°, называется температурным коэффициентом скорости реакции - γ.
Это правило математически выражается следующей формулой:
![]() (12)
(12)
где γ - температурный коэффициент, который показывает, во сколько раз увеличивается скорость реакции при повышении температуры на 10 0 ; υ 1 – t 1 ; υ 2 – скорость реакции при температуре t 2 .
При повышении температуры в арифметической прогрессии скорость возрастает в геометрической.
Например, если γ = 2,9, то при возрастании температуры на 100° скорость реакции увеличивается в 2,9 10 раз, т.е. в 40 тыс. раз. Отклонения от этого правила составляют биохимические реакции, скорость которых увеличивается в десятки раз при незначительном повышении температуры. Это правило справедливо лишь в грубом приближении. Реакции, в которых участвуют крупные молекулы (белка), характеризуются большим температурным коэффициентом. Скорость денатурации белка (яичного альбумина) возрастает в 50 раз при повышении температуры на 10 °С. После достижения некоторого максимума (50-60 °С) скорость реакции резко понижается в результате термоденатурации белка.
Для многих химических реакций закон действующих масс для скорости неизвестен. В таких случаях для описания температурной зависимости скорости превращения может применяться выражение:
Предэкспонента А с не зависит от температуры, однако зависит от концентрации. Единицей измерения является моль/л∙с.
Теоретическая зависимость позволяет заранее рассчитывать скорость при любой температуре, если известны энергия активации и предэкспонента. Таким образом, прогнозируется влияние температуры на быстроту протекания химического превращения.
Сложные реакции
Принцип независимости. Все рассмотренное выше относилось к сравнительно простым реакциям, но в химии часто встречаются так называемые сложные реакции. К таким реакциям относятся рассматриваемые ниже. При выводе кинетических уравнений для этих реакций используют принцип независимости: если в системе протекает несколько реакций, то каждая из них независима от других и ее скорость пропорциональна произведению концентраций ее реагентов.
Параллельные реакции - это реакции, идущие одновременно в нескольких направлениях.
Термический распад хлората калия протекает одновременно по двум реакциям: ![]()
Последовательные реакции - это реакции, которые протекают в несколько стадий. Таких реакций в химии большинство.
![]() .
.
Сопряженные реакции. Если в системе протекают несколько реакций и протекание одной из них невозможно без другой, то эти реакции называются сопряженными , а само явление - индукцией .
2HI + Н 2 СrО 4 → I 2 + Сr 2 О 3 + Н 2 О.
Эта реакция в обычных условиях практически не наблюдается, но если в систему добавить FеО, то происходит реакция:
FеО + Н 2 СrО 4 → Fе 2 О 3 + Сr 2 O 3 + Н 2 О
и одновременно с ней идет первая реакция. Причиной этого является образование во второй реакции промежуточных продуктов, участвующих в первой реакции:
FеО 2 + Н 2 СrО 4 → Сr 2 О 3 + Fе 5+ ;
HI + Fе 5+ → Fе 2 О 3 + I 2 + Н 2 О.
Химическая индукция - явление, при котором одна химическая реакция (вторичная) зависит от другой (первичной).
А + В - первичная реакция,
А + С - вторичная реакция,
то А - активатор, В - индуктор, С - акцептор.
При химической индукции, в отличие от катализa, концентрации всех участников реакции уменьшаются.
Фактор индукции определяется из следующего уравнения:
![]() .
.
В зависимости от величины фактора индукции возможны следующие случаи.
I > 0 - затухающий процесс. Скорость реакции снижается со временем.
I < 0 - ускоряющийся процесс. Скорость реакции увеличивается со временем.
Явление индукции важно тем, что в ряде случаев энергия первичной реакции может скомпенсировать затраты энергии во вторичной реакции. По этой причине, например, оказывается термодинамически возможным синтез белков путем поликонденсации аминокислот.
Цепные реакции. Если химическая реакция протекает с образованием активных частиц (ионов, радикалов), которые, вступая в последующие реакции, вызывают появление новых активных частиц, то такая последовательность реакций называется цепной реакцией .
Образование свободных радикалов связано с затратой энергии на разрыв связей в молекуле. Эта энергия может быть сообщена молекулам путем освещения, электрического разряда, нагревания, облучения нейтронами, α- и β-частицами. Для проведения цепных реакций при невысоких температурах в реагирующую смесь вводят инициаторы - вещества, легко образующие радикалы: пары натрия, органические пероксиды, иод и т. д.
Реакция образования хлороводорода из простых соединений, активируемая светом.
Суммарная реакция:
Н 2 + С1 2 2НС1.
Отдельные стадии:
Сl 2 2Сl∙ фотоактивация хлора (инициирование)
Сl∙ + Н 2 = НСl + Н∙ развитие цепи
Н∙ + Сl 2 = НСl + Сl∙ и т. д.
Н∙ + Сl∙ = НСl обрыв цепи
Здесь Н∙ и Сl∙ - активные частицы (радикалы).
В этом механизме реакции можно выделить три группы элементарных стадий. Первая представляет собой фотохимическую реакцию зарождения цепи . Молекулы хлора, поглотив квант света, диссоциируют на свободные атомы, обладающие высокой реакционной способностью. Таким образом, при зарождении цепи происходит образование свободных атомов или радикалов из валентно-насыщенных молекул. Процесс зарождения цепи называют также инициированием . Атомы хлора, обладая непарными электронами, способны реагировать с молекулярным водородом, образуя молекулы хлороводорода и атомарного водорода. Атомарный водород, в свою очередь, вступает во взаимодействие с молекулой хлора, в результате чего снова образуется молекула хлороводорода и атомарный хлор и т. д.
Эти процессы, характеризующиеся повторением одних и тех же элементарных стадий (звеньев) и идущие с сохранением свободных радикалов, приводят к расходованию исходных веществ и образованию продуктов реакции. Такие группы реакций называют реакциями развития (или продолжения) цепи.
Стадия цепной реакции, при которой происходит гибель свободных радикалов, называется обрывом цепи . Обрыв цепи может наступить в результате рекомбинации свободных радикалов, если выделяющаяся при этом энергия может быть отдана какому-либо третьему телу: стенке сосуда или молекулам инертных примесей (стадии 4, 5). Вот почему скорость цепных реакций очень чувствительна к наличию примесей, к форме и размерам сосуда, особенно при малых давлениях.
Число элементарных звеньев от момента зарождения цепи до ее обрыва называют длиной цепи. В рассматриваемом примере на каждый квант света образуется до 10 5 молекул НСl.
Цепные реакции, в ходе которых не происходит «умножения» числа свободных радикалов, называются неразветвленными или простыми цепными реакциями . В каждой элементарной стадии неразветвленного цепного процесса один радикал «рождает» одну молекулу продукта реакции и только один новый радикал (рис. 41).
| |
Другие примеры простых цепных реакций: а) хлорирование парафиновых углеводородов Сl∙ + СН 4 → СН 3 ∙ + НС1; СН 3 ∙ + Сl - → СН 3 Сl + Сl∙ и т. д.; б) реакции радикальной полимеризации, например, полимеризация винилацетата в присутствии перекиси бензоила, легко распадающегося на радикалы; в) взаимодействие водорода с бромом, протекающее по механизму, аналогичному при реакции хлора с водородом, только с меньшей длиной цепи вследствие ее эндотермичности.
Если в результате акта роста появляются две или более активных частиц, то эта цепная реакция является разветвленной.
В 1925 г. Н. Н. Семенов и его сотрудники открыли реакции, содержащие элементарные стадии, в результате которых возникают не одна, а несколько химически активных частиц - атомов, или радикалов. Появление нескольких новых свободных радикалов приводит к появлению нескольких новых цепей, т.е. одна цепь разветвляется. Такие процессы называют разветвленными цепными реакциями (рис. 42).
Примером сильно разветвленного цепного процесса является реакция окисления водорода при низких давлениях и температуре около 900°С. Механизм реакции можно записать так.
1. H 2 + O 2 OH∙ + OH∙ зарождение цепи
2. ОН∙ + Н 2 → Н 2 О + Н∙ развитие цепи
3. Н∙ + О 2 → ОН∙ + О: разветвление цепи
4. О: + Н 2 → ОН∙ +Н∙
5. ОН∙ +Н 2 → Н 2 О + Н∙ продолжение цепи
6. Н∙ + Н∙ + стенка → Н 2 обрыв цепи на стенке сосуда
7. Н∙ + О 2 + М → НО 2 ∙ + М обрыв цепи в объеме.
М - инертная молекула. Радикал НО 2 ∙, образующийся при тройном соударении, малоактивен и не может продолжать цепь.
На первой стадии процесса образуются радикалы гидроксила, которые обеспечивают развитие простой цепи. В третьей же стадии в результате взаимодействия с исходной молекулой одного радикала образуются два радикала, причем атом кислорода обладает двумя свободными валентностями. Это и обеспечивает разветвление цепи.
В результате разветвления цепи скорость реакции в начальный период времени стремительно нарастает, и процесс заканчивается цепным воспламенением-взрывом. Однако разветвленные цепные реакции заканчиваются взрывом только в том случае, когда скорость разветвления больше скорости обрыва цепей. В противном случае наблюдается медленное течение процесса.
При изменении условий протекания реакции (изменение давления, температуры, состава смеси, размера и состояния стенок реакционного сосуда и т. д.) может произойти переход от медленного течения реакции к взрыву и наоборот. Таким образом, з цепных реакциях существуют предельные (критические) состояния, при которых происходит цепное воспламенение, от которого следует отличать тепловое воспламенение, возникающее в экзотермических реакциях в результате все увеличивающегося разогревания реагируемой смеси при слабом теплоотводе.
По разветвленному цепному механизму происходит окисле-кие паров серы, фосфора, оксида углерода (II), сероуглерода и т. д.
Современная теория цепных процессов разработана лауреатами Нобелевской премии (1956) советским академиком Н. Н. Семеновым и английским ученым Хиншельвудом.
Цепные реакции следует отличать от реакций каталитических, хотя последние носят и циклический характер. Самое существенное отличие цепных реакций от каталитических заключается в том, что при цепном механизме возможно течение реакции в направлении повышения энергии системы за счет самопроизвольно протекающих. Катализатор же термодинамически невозможную реакцию не вызывает. Кроме того, в каталитических реакциях отсутствуют такие стадии процесса, как зарождение и обрыв цепи.
Реакции полимеризации. Частный случай цепной реакции - реакция полимеризации.
Полимеризацией называется процесс, при котором реакция активных частиц (радикалов, ионов) с низкомолекулярными соединениями (мономерами) сопровождается последовательным присоединением последних с увеличением длины материальной цепи (длины молекулы), т. е. с образованием полимера.
Мономерами являются органические соединения, как правило, содержащие в составе молекулы непредельные (двойные, тройные) связи.
Основные стадии процесса полимеризации:
1. Инициирование (под действием света, нагревания и т. д.):
А: А → А" + А" - гомолитический распад с образованием радикалов (активные валентноненасыщенные частицы).
А: В → А - + В + - гетеролитический распад с образованием ионов.
2. Рост цепи: А" + М → АМ"
(или А - + М → АМ", или В + + М → ВМ +).
3. Обрыв цепи: АМ" + АМ" → полимер
(или АМ" + В + → полимер, ВМ + + А" → полимер).
Скорость цепного процесса всегда больше, чем нецепного.